Владельцы патента RU 2355413:
Изобретение относится к медицине и фармакологии и представляет собой средство для лечения демиелинизирующих заболеваний нервной системы, содержащее стефаглабрина сульфат, который способствует восстановлению миелиновой оболочки нервного волокна, применение его и способ лечения. Изобретение обеспечивает повышение эффективности лечебного действия средства, возможность применения его в низких дозах, уменьшение числа побочных эффектов, ускорение и повышение эффективности лечения демиелинизирующих заболеваний нервной системы. 3 н. и 2 з.п. ф-лы.
Изобретение относится к области фармакологии и касается фармацевтических средств, используемых при лечении неврологических заболеваний, в частности демиелинизирующих заболеваний нервной системы, и может быть использовано при лечении деструктивных и дегенеративно-дистрофических заболеваний, например, таких как острые и хронические полирадикулоневропатии, полиневропатии с блоком проведения дисметаболических и токсических невропатий, невропатий и невралгий черепно-мозговых нервов, туннельных невропатий и т.п.
Основными функциональными элементами нервной системы являются нервные клетки или нейроны, составляющие 10-15% общего числа клеточных элементов в нервной системе. Остальную, большую ее часть ее занимают клетки нейроглии.
Функция нейронов заключается в восприятии сигналов от рецепторов или других нервных клеток, хранении и переработке информации и передаче нервных импульсов к другим клеткам - нервным, мышечным или секреторным. Составляющие основную массу нервной ткани глиальные элементы выполняют вспомогательные функции и заполняют почти все пространство между нейронами. Анатомически среди них различают клетки нейроглии в мозге (олигодендроциты и астроциты) и шванновские клетки в периферической нервной системе. Олигодендроциты и шванновские клетки формируют вокруг аксонов (отростков нервной клетки) миелиновые оболочки.
Миелин - особый вид клеточной мембраны, окружающей отростки нервных клеток, в основном аксоны, в центральной и периферической нервной системах. По химическому составу миелин - это липопротеидная мембрана, состоящая из биомолекулярного липидного слоя, расположенного между мономолекулярными слоями белков, спирально закрученная вокруг интернодального сегмента нервного волокна. Основные функции миелина: метаболическая изоляция и ускорение проведения нервного импульса, а также опорная и барьерная функции.
Заболевания, одним из основных проявлений которых является деструкция нервных волокон и разрушение миелина, в настоящее время являются одной из наиболее актуальных проблем клинической медицины, преимущественно неврологии. В последние годы наблюдается отчетливое увеличение числа случаев заболеваний, сопровождающихся повреждением миелина. Много книг, полезных материалов по медицине, в том числе заболеваниям нервной системы можно найти на сайте skladchik.com . Информация достается совсем недорого, потому что приобретается методом коллективных покупок.
Разрушение миелина может быть связано с биохимическими дефектами его строения, которые, как правило, являются генетически детерминированными или обусловленными повреждением нормально синтезированного миелина под влиянием различных воздействий.
Разрушение миелина является универсальным механизмом реакции нервной ткани на ее повреждение. Нервные болезни, связанные с деструкцией миелина, можно разделить на две основные группы - миелинопатии и миелинокластии. Большинство миелинопатий связано с наследственными заболеваниями, приводящими к генетически обсловленным биохимическим дефектам строения миелина. В основе миелинокластических заболеваний лежит разрушение нормально синтезированного миелина под влиянием различных воздействий, как внешних, так и внутренних. Подразделение рассматриваемых заболеваний на эти две группы весьма условно, так как первые клинические проявления миелинопатий могут быть связаны с воздействием различных внешних факторов, а миелинокластии вероятнее всего развиваются у предрасположенных лиц.
Примером наследственных миелинопатий могут служить адренолейкодистрофии (АЛД), которые связаны с недостаточностью функции коры надпочечников и характеризуются активной диффузной демиелинизацией различных отделов как центральной, так и периферической нервной системы.
Основной метаболический дефект при этом заболевании - увеличение содержания в тканях насыщенных жирных кислот с длинной цепью (особенно С-26), что приводит к грубым нарушениям структуры и функций миелина. Клинические проявления: нарастающая слабость в ногах, нарушение чувствительности по полиневротическому типу ("носки" и "перчатки"), нарушения координации. Эффективного специфического лечения АЛД в настоящее время не существует, поэтому проводится симптоматическая терапия.
Описана поздняя форма суданофильной лейкодистрофии Пелицеуса-Мерцбахера с началом заболевания на втором десятилетии жизни. Выраженное демиелинизирующее поражение головного мозга у этих больных сопровождается снижением содержания эфиров холестерина. У этих больных прогрессивно нарастают нарушения координации, спастические парезы, интеллектуальные нарушения.
Группа лейкодистрофии характеризуется демиелинизацией с диффузной волокнистой дегенерацией белого вещества головного мозга и образованием в ткани мозга глобоидных клеток. Среди них особого интереса заслуживает болезнь Александера - редкое заболевание, преимущественно наследуемое по аутосомно-рецессивному типу. Эта дисмиелинопатия характеризуется тем, что в миелине вместо галактолипидов и цереброзидов накапливаются глюколипиды. Для нее характерны постепенно нарастающие спастические параличи, снижение остроты зрения и деменция, эпилептический синдром, гидроцефалия.
К группе глобоидо-клеточных лейкодистрофий относятся и такие редкие заболевания, как болезнь Краббе и болезнь Канавана. Эти заболевания редко развиваются во взрослом возрасте. Клинически они характеризуются прогрессирующим поражением миелина разных отделов ЦНС с развитием парезов, нарушений координации, деменции, слепоты, эпилептическим синдромом.
Среди миелинокластических заболеваний особого внимания заслуживают вирусные инфекции, в патогенезе которых важную роль играет разрушение миелина. Это в первую очередь нейроСПИД, вызываемый вирусом иммунодефицита человека (ВИЧ), и связанные с ним поражения нервной системы, а также тропический спинальный парапарез (ТСП), вызываемый ретровирусом HTLV-I.
Патогенез первичного поражения ЦНС при указанных вирусных заболеваниях связан с непосредственным нейротоксическим воздействием вирусов, а также с патологическим действием цитотоксических Т-клеток, антител и нейротоксических веществ, вырабатываемых инфицированными иммуноцитами. Прямое поражение мозга при ВИЧ-инфекции приводит к развитию подострого энцефалита с участками демиелинизации.
Лечение всех вирусных инфекций основано на использовании противовирусных препаратов, останавливающих размножение вируса в инфицированных клетках.
У лиц с кахексией, страдающих хроническим алкоголизмом, тяжелыми хроническими заболеваниями печени и почек, при диабетическом кетоацидозе, во время проведения реанимационных мероприятий может развиваться тяжелое демиелинизирующее заболевание - острый или подострый центральный понтийный и/или экстрапонтийный миелинолиз. При этом заболевании симметричные билатеральные очаги демиелинизации образуются в подкорковых узлах и стволе головного мозга. Предполагается, что основой этого процесса является нарушение баланса электролитов, в первую очередь ионов Na. Особенно высок риск развития миелинолиза при быстрой коррекции гипонатрийемии. Клинически этот синдром может проявляться как минимальными неврологическими симптомами, так и тяжелыми альтернирующими синдромами и развитием комы. Заболевание обычно через несколько недель заканчивается смертью, но в ряде случаев массивные дозы кортикостероидов предотвращают летальный исход.
После химио- и лучевой терапии может развиваться токсическая лейкоэнцефалопатия с очаговой демиелинизацией в сочетании с мультифокальным некрозом. Возможно развитие острых, ранних отсроченных и поздних демиелинизирующих процессов. Последние начинаются через несколько месяцев или лет после облучения и характеризуются тяжелым течением с полиморфной очаговой неврологической симптоматикой. В патогенезе этих заболеваний существенное значение имеют аутоиммунные реакции на антигены миелина, повреждение олигодендроцитов и, следовательно, нарушение процессов ремиелинизации. Токсическое повреждение миелина может наблюдаться также при порфирии, гипотиреозе, интоксикациях ртутью, свинцом, СО, цианидами, при всех видах кахексии, передозировке антиконвульсантов, изониазида, актиномицина, при героиновой и морфиновой наркоманиях.
Особого внимания заслуживает ряд миелинокластических заболеваний, которые могут рассматриваться как особые варианты рассеянного склероза.
Концентрический склероз, или болезнь Балло, является неуклонно прогрессирующим демиелинизирующим заболеванием лиц молодого возраста. При этом заболевании образуются большие очаги демиелинизации преимущественно в белом веществе лобных долей, иногда с вовлечением серого вещества. Очаги состоят из чередующихся областей полной и частичной демиелинизации с выраженным ранним поражением олигодендроцитов.
Следует отметить, что очаги демиелинизации в ЦНС довольно часто выявляются у больных с системной красной волчанкой, первичным синдромом Шегрена с васкулитами различного генеза и другими системными аутоиммунными заболеваниями. Разрушение миелина и развитие аутоиммунных реакций на его компоненты наблюдается при многих сосудистых и паранеопластических процессах в ЦНС (Е.И.Гусев, А.Н.Бойко. Демиелинизирующие заболевания центральной нервной системы, Consilium-Medicum, Том 2, N2, 2000).
Лечение, направленное на замедление или остановку прогрессирования заболеваний, сопровождающихся демиелинизацией, в основном основано на представлениях о них как аутоиммунных заболеваниях. Аутоиммунный процесс сопровождается появлением миелинотоксических антител и Т-лимфоцитов-киллеров, разрушающих шванновские клетки и миелин. Для коррекции иммунной системы применяют иммуносупрессоры, снижающие активность иммунной системы, и иммуномодуляторы, изменяющие соотношение компонентов иммунной системы. Иммуносупрессия и иммуномодуляция направлены на разрушение, удаление или изменение функции лимфоцитов, способных повреждать миелин.
Среди методов, влияющих на аутоиммунные механизмы заболевания, предпочтение отдается плазмаферезу, внутривенному введению человеческого IgG и применению кортикостероидов (Невропатии. Под редакцией Н.М.Жулева, Санкт-Петербург, 2005 г.).
Однако плазмаферез может быть осуществлен только в больничных условиях, и его применение у пациентов, сохранивших способность к самостоятельному перемещению, не всегда является оправданным.
Противопоказаниями для назначения IgG являются наличие анафилактических реакций, сердечная и почечная недостаточность. Осложнения отмечаются примерно у 10% пациентов.
При назначении кортикостероидной терапии учитывается наличие общеизвестных противопоказаний (язвенная болезнь желудка и двенадцатиперстной кишки, высокая артериальная гипертензия, диабет и др.), и должны применяться средства, предупреждающие развитие наиболее частых осложнений (препараты калия, аскорбиновая кислота, рутин и т.п.).
В литературе содержится упоминание о препарате неинтерфероновой природы - копаксоне (Сорахопе-Теуа) (международное название - глатирамера ацетат). Копаксон является уксусно-кислой солью синтетических полипептидов, образованных 4 природными аминокислотами: L-глутаминовой кислотой, L-аланином, L-тирозином и L-лизином и по химическому строению имеет элементы сходства с основным белком миелина. Относится к классу иммуномодуляторов и обладает способностью блокировать миелин-специфические аутоиммунные реакции, лежащие в основе разрушения миелиновой оболочки нервных волокон при рассеянном склерозе. Однако при клиническом применении препарата отмечены многочисленные побочные реакции (абсцессы и гематомы в месте введения, повышение артериального давления, спленомегалия, аллергические реакции, апафилаксия, артриты, головная боль, депрессия, судороги, бронхоспазм, импотенция, аменорея, гематурия и др.) (Хохлов А.П., Савченко Ю.Н. «Миелинопатии и демиелинизирующие заболевания», М., 1991 г.).
По данным литературы, известно применение препаратов из лекарственных растений, которые предупреждают развитие демиелинизации нейронов - это различные препараты подорожника, топинамбура, цикория, одуванчика, спорыша, пырея, тыквы, бессмертника, подорожника; полифитохол, полиспонин, сибектан, хитохол, хитолен, сирепар, тыквеол, тыквейнол, розоптин (Корсун В.Ф., Корсун Е.В. Лекарственные растения в лечении рассеянного склероза: Методическое пособие. - М.: «ИНФИТ». -2004).
Известен стефаглабрин сульфат (Stphaglabrini sulfas) - сульфат алкалоида стефарина, выделенного из клубней с корнями стефании гладкой - (Stephania glabra (Rob) Miers, сем. луносемянниковых (Menispermaceae)) многолетнего тропического травянистого растения семейства мениспермовых. Произрастает в субтропических и тропических горных районах Южного Китая, Японии, Бирмы, Вьетнама, Индии. В СССР были предприняты попытки интродукции данного растения в субтропиках Закавказья, однако они успеха не имели. Основная масса сырья импортируется из Индии. Известен также способ получения стефаглабрина из растительного сырья (авторское свидетельство СССР №315387, 1963 г.).
Известно получение линии Stephania glabra в суспензионной культуре, с высоким уровнем синтеза алкалоида стефарина. Культура in vitro Stephania glabra была получена в Институте лекарственных растений (ВИЛАР). Разработка системы селекции in vitro проводилась в ИФРе.
Лекарственный препарат стефаглабрина сульфат - сернокислая соль алкалоида стефарина - (C 18 H 19 O 3 N 2) 2 ·H 2 SO 4 относится к производным проапорфина.
Представляет собой белый кристаллический порошок с температурой плавления 245-246°С (в вакууме), хорошо растворимый в воде и водном спирте. Стефаглабрин сульфат угнетает активность истинной и ложной холинэстеразы, оказывает тонизирующее действие на гладкую мускулатуру и снижает артериальное давление. Малотоксичен.
Ранее было разрешено использование стефаглабрина сульфата в медицинской практике в качестве антихолиноэстеразного средства (авторское свидетельство СССР №315388, 1963 г.).
Дальнейшие исследования авторов показали, что стефаглабрин сульфат обладает специфической ингибирующей активностью на развитие соединительной ткани, предотвращая образование рубца при повреждении нерва, и может быть применен в качестве средства для лечения травматических и послеоперационных повреждений периферической нервной системы (патент СССР №1713151, 1985 г.).
Неожиданным, подтвержденным в экспериментах, оказалось выявленное авторами свойство стефаглабрина сульфата стимулировать рост шванновских клеток и последующее образование миелина, по-видимому, под влиянием нейроростовых факторов, образующихся под действием препарата, что способствует восстановлению миелиновой оболочки нервного волокна и, таким образом, восстановлению его функционального состояния, нарушенного в результате поражения нервной системы (аксональной дегенерации, аутоиммунной сегментарной демиелинизации и первичной сегментарной демиелинизации).
Задачей настоящего изобретения является создание эффективного и с минимальными побочными эффектами фармацевтического средства для лечения деструктивных и демиелинизирующих заболеваний нервной системы, выявление нового применения стефаглабрина сульфата и создание способа лечения деструктивных и демиелинизирующих заболеваний нервной системы.
Для решения этой задачи авторами предложено фармацевтическое средство для лечения деструктивных и демиелинизирующих заболеваний нервной системы, содержащее стефаглабрин сульфат в качестве средства, способствующего восстановлению миелиновой оболочки нервного волокна, при этом содержание стефаглабрина сульфата в нем составляет от 0,2 до 1,0%; применение стефаглабрина сульфата при лечении деструктивных и демиелинизирующих заболеваний нервной системы в качестве средства, способствующего восстановлению миелиновой оболочки нервного волокна, и способ лечения деструктивных и демиелинизирующих заболеваний нервной системы, включающий симптоматическую терапию и электрофизиологические процедуры, при этом пациенту дополнительно назначают стефаглабрин сульфат в качестве ремиелинизирующего средства. Стефаглабрин сульфат вводят пациенту парентерально по 2-8 мл 0,25% раствора 2 раза в день. Курс лечения 20 дней.
Технический результат предложенной совокупности объектов заключается в высокой эффективности лечебного действия препарата при использовании его в низких дозах, уменьшении числа нежелательных побочных эффектов, а также в ускорении и повышении эффективности лечения деструктивных и демиелинизирующих заболеваний нервной системы.
В экспериментах на крысах было установлено, что под влиянием стефаглабрина сульфата в диапазоне наиболее оптимальных доз от 0,1 и до 1,0 мг/кг рано начинается миелинизация дегенерирующих нервов, идет значительно быстрее и полнее, заканчивается в более ранние сроки по сравнению с животными, не получавшими препарат.
К 60-80 суткам у леченных стефаглабрином сульфатом крыс большинство нервных волокон в периферических концах нервов имело миелиновое покрытие и нормальное гистологическое строение. Проведенные электрофизиологические исследования показали полное восстановление скорости проведения импульса по нерву.
В то время как у контрольных животных, не получавших лечение стефаглабрином сульфатом, миелинизация нервных волокон проходила медленно и полностью не завершалась даже к 100-120 суткам.
Следующие примеры поясняют сущность изобретения, не ограничивая его.
Применение стефаглабрина сульфата внутримышечно по 2,0 мл 0,25% раствора 2 раза в сутки в течение 2-3 недель было эффективным при лечении больных миелопатией с элементами бокового амиотрофического синдрома. При этом отмечалось исчезновение фибрилляций, уменьшение выраженности амиотрофий и поликинетичности проприоцептивных рефлексов, нарастание мышечной силы в руках.
Препарат был эффективен у больных цереброспинальной формой рассеянного склероза с тетрапарезом, мозжечково-атактическим синдромом и тазовыми расстройствами.
Препарт применяли у 37 больных сирингомиелией. Положительный эффект отмечен у 28 больных: уменьшилась интенсивность болей вплоть до их исчезновения к 10-14 дню применения препарата, восстанавливалась чувствительность на лице с появлением корнеальных рефлексов, ликвидировались расстройства глотания, а также отмечалось восстановление чувствительности (болевая и температурная) на туловище и конечностях.
Наилучший терапевтический эффект отмечен в группе больных, которым стефаглабрин сульфат вводили внутримышечно по 2 мл 2 раза в день (на курс 100-200 ампул). Наряду с применением препарата всем больным назначали массаж, лечебную физкультуру, ионизацию позвоночника с калия иодидом, витамины В 1 , В 12 . Следует отметить, что через 2-3 недели после начала лечения снижались границы чувствительных нарушений. Особого внимания заслуживает восстановление нарушенных функций у больных с начальными явлениями сирингобульбии. У ряда больных наблюдалось уменьшение интенсивности (вплоть до исчезновения) болей симпаталгического характера, которое наступало на 10-12 день применения препарата.
Положительный терапевтический эффект был отмечен при применении стефаглабрина сульфата у 14 больных с тяжелым боковым амиотрофическим склерозом. В результате лечения у 12 больных отмечены нарастание силы в конечностях, уменьшение расстройства бульбарных функций - глотания и дыхания.
Так, у одного больного боковым амиотрофическим склерозом, сопровождающимся афонией, дисфагией, после инъекций стефаглабрина сульфата по 2 мл 2 раза в день в течение 10 дней заметно улучшилось глотание.
У другого больного восстановилось нарушенное дыхание, которое не поддавалось лечению другими препаратами.
1. Фармацевтическое средство для лечения демиелинизирующих заболеваний нервной системы, характеризующееся тем, что оно содержит стефаглабрина сульфат, способствующий восстановлению миелиновой оболочки нервного волокна.
2. Фармацевтическое средство по п.1, характеризующееся тем, что содержание стефаглабрина сульфата в нем составляет от 0,2 до 1,0%.
3. Применение стефаглабрина сульфата для получения средства, способствующего восстановлению миелиновой оболочки нервного волокна.
4. Способ лечения демиелинизирующих заболеваний нервной системы, включающий симптоматическую терапию и электрофизиологические процедуры, отличающийся тем, что пациенту дополнительно вводят 0,25%-ный раствор стефаглабрина сульфата парентерально.
Системные повреждения периферических нервов (полиневропатии) и повреждения отдельных нервных стволов (невропатии) составляют большую группу заболеваний периферической нервной системы различной этиологии и сложного патогенеза, приводящих к разрушению нервных волокон или их оболочек. Распространенность патологических процессов, протекающих с повреждением периферических нервов настолько велика, что большая часть обращений пациентов к неврологу связана именно с ними.
Международная статистическая классификация болезней (МКБ-10) содержит огромный раздел (G 50 - 64), который включает в себя все многообразие клинических вариантов невропатий: от поражения отдельных нервов, корешков и сплетений до системных полиневропатий.
Повреждения периферических нервов может быть обусловлено обменными нарушениями, ишемией, заболеваниями крови, интоксикациями, алиментарными факторами, травмами, аллергическими реакциями, воспалительными процессами и другими причинами.
Страдания образований периферической нервной системы выступают как самостоятельное заболевание или клинический синдром и так часто встречаются в практике врача, что ни один специалист как терапевтического, так и хирургического профиля не может пройти мимо этой проблемы.
К периферической нервной системе относится задние и передние корешки спинного мозга, межпозвоночные спинальные ганглии, спинномозговые нервы, их сплетения, периферические нервы, а также корешки и ганглии черепных нервов и черепные нервы.
Формирование периферического нерва происходит следующим образом. Следуя на периферию из спинного мозга (или из полости черепа), спинальные нервы (или черепные нервы), состоящие из порций двигательных, чувствительных волокон, образуют периферический нерв. Периферические нервы являются в большинстве своем смешанными и состоят из двигательных волокон передних корешков (аксонов клеток передних рогов), чувствительных волокон (дендритов клеток межпозвонковых узлов) и вазомоторно-секреторно-трофических волокон (симпатических и парасимпатических) от соответствующих клеток серого вещества боковых рогов спинного мозга и ганглиев симпатического пограничного ствола.
Нервное волокно, входящее в состав периферического нерва, состоит из осевого цилиндра, расположенного в центре волокна, миелиновой оболочки, одевающей осевой цилиндр и швановской оболочки. Крупные нервные стволы состоят из 800 000 – 1 000 000 нервных волокон, которые обеспечивают значительный функциональный запас прочности периферической нервной системы. Считается, что функция нервного ствола нарушается только в случае гибели половины нервных волокон.

Миелиновая оболочка нервного волокна местами прерывается, образуя так называемые перехваты Равнье. Долгие годы считалось, что миелиновая оболочка обеспечивает роль электрического изолятора в процессе проведения возбуждения по нервному волокну. Однако, роль миелиновой оболочки, вероятно, более значительна – она принимает непосредственное участие в формировании электрического потенциала нервного волокна. Несомненно, ее участие в процессах обмена веществ нервной клетки чрезвычайно велико – функция нервного волокна нарушается при повреждении миелиновой оболочки. Соединительная ткань в периферических нервах представлена оболочками, одевающими нервный ствол (эпиневрий), отдельные его пучки (периневрий) и нервные волокна (эндоневрий). В оболочках проходят сосуды, питающие нерв. Миелиновая оболочка составляет основную массу периферического нерва.
Миелин – вещество, состоящее из холестерина, фосфолипидов и белков – результат фолат-зависимого синтеза, протекающего при непосредственном участии фермента метилентетрагидрофолатредуктазы (МТГФР) и коферментов (фолиевая кислота и витамины группы В).
Миелиновая оболочка – наиболее уязвимая часть периферического нерва. Она страдает в результате разрушения (токсические, иммунные механизмы) или недостаточного синтеза составляющих миелина (обменные нарушения, недостаток витаминов). В любом случае синтез миелина требует существенного напряжения многочисленных ферментных систем, поскольку общая масса этого вещества в организме превышает 200 гр.
Клинический синдром повреждения периферических нервов чаще всего связан с сегментарной демиелинизацией нервных волокон. Сегментарная демиелинизация (миелинопатия) означает повреждение миелиновых оболочек при сохранности аксонов. Наиболее существенным функциональным проявлением демиелинизации является блокада проводимости. Функциональная недостаточность в блокированном аксоне проявляется также, как и при пересечении аксона. Несмотря на то, что пересечение нерва и блокада проводимости при демиелинизации обнаруживают сходство по остроте развития двигательных и чувствительных расстройств, между ними имеются различия. Так при демиелинизирующих невропатиях блокада проводимости часто бывает преходящей и ремиелинизация может протекать быстро в течение дней или недель, нередко заканчиваясь выздоровлением (4). Таким образом, при этом процессе прогноз благоприятнее и восстановление идет быстрее, нежели течение. Важнейшим клиническим признаком сегментарной демиелинизации является расстройство функции по дистально-периферическому типу – чем больше протяженность периферического нерва, тем более заметными становятся нарушения проводимости. Прежде всего, это проявляется расстройствами чувствительности в дистальных отделах конечностей.
Итак, фолат-зависимый синтез миелина невозможен без витаминов группы В. Между тем, недостаток тиамина (витамин В1) считается одной из характерных черт типичных болезней цивилизации (5). Изменения характера питания с увеличением доли рафинированных углеводов, значительное закисление внутренней среды вследствие изменения структуры продуктов питания – не способствуют усвоению тиамина, даже если он в достаточном количестве присутствует в пище. Между тем В1 принимает участие в белковом синтезе, регуляции жирового и водно-солевого обмена. Многочисленными исследованиями установлено, что тиамин обладает антиоксидантными, иммуномодулирующими свойствами, участвует в метаболизме важнейших нейромедиаторов – серотонина и гамма-аминомасляной кислоты, ацетилхолина. Являясь основным коферментом МТГФР, он принимает непосредственное участие в синтезе миелина.
Витамин В6 – пиридоксин является коферментом более 100 ферментов, принимает участие в синтезе нейромедиаторов (триптофан, глицин, серотонин, дофамин, норадреналин, адреналин, гистамин). Он снижает уровень холестерина, гомоцистеина в крови. Витамин В6 контролирует эритропоэз и участвует в формировании иммунного ответа. Существует убедительная корреляция между снижением уровня пиридоксина в крови и клиническими проявлениями полиневропатий.
Витамин В12 (цианкобаламин) – основной источник кобальта, необходимого в процессах синтеза белка. В12 принимает непосредственное участие в синтезе метионина и нуклеиновых кислот. Он активирует все виды обмена веществ: белковый, жировой и углеводный. Установлено, что высокие концентрации цианкобаламина необходимы для предотвращения когнитивных нарушений (старческого слабоумия), депрессии. Участие В12 в синтезе миелина является его важнейшей функцией. Комплексные витаминные препараты нашли широкое применение в лечении больных с различными заболеваниями и патологическими процессами. Но наиболее значимо их применение при заболеваниях нервной системы. Не случайно витамины группы В заняли центральное место в лечении заболеваний периферической нервной системы. Среди многочисленных болезней нервной системы наиболее значимы показания для витаминных препаратов при полиневропатиях различного генеза (1 - 3). Хотя этиология полиневропатий крайне разнообразна, недостаток витаминов группы В объединяет большинство клинических вариантов этого неврологического синдрома. Согласно литературным данным, полиневропатии, возникающие вследствие осложнений сахарного диабета или алкогольной интоксикации, составляют более двух третей всех случаев полиневропатий (1). Современные исследования демонстрируют, что у пациентов, страдающих сахарным диабетом, дефицит тиамина развивается вследствие его повышенного выведения почками. Восполнение тиамина для больных сахарными диабетом является задачей повседневной практики. Установлено, что назначение тиамина в дозе около 300 мг в сутки в комплексе с витаминами В6 и В12 существенно уменьшает или устраняет проявления полиневропатии, в первую очередь, уменьшая нейропатическую боль (2). Помимо уменьшения проявлений расстройств чувствительности витамины при полиневропатии оказывают существенное влияние на проявления вегетативно-трофических нарушений при нейропатической форме синдрома диабетической стопы.
Системные нарушения обмена, протекающие с ожирением, в последние годы привлекают все большее внимание врачей. Оперативное лечение морбидного ожирения становится все более распространенной практикой. Оперативная реконструкция желудочно-кишечного тракта часто спасает пациентов от ряда фатальных осложнений. Однако, в последующем, в результате нарушения процесса усвоения биологически важных веществ, нередко больные страдают от нарушений со стороны периферической нервной системы. Пациенты, после хирургических операций по поводу морбидного ожирения требуют компенсирующего лечения с обязательным включением витаминов группы В в течение всего периоды реабилитации. Основной целью назначения витаминных препаратов в этом случае является предотвращение дисметаболических полиневропатий.
Острые воспалительные демиелинизирующие полиневропатии требуют парентерального введения витаминов группы В как в остром, так и восстановительном периоде. При этом для активации синтеза миелина необходима комбинация витаминов группы В с фолиевой кислотой (4).
Недостаток витаминов группы В при алкогольной полиневропатии обусловлен как минимум тремя факторами. Этиловый спирт ингибирует процесс фосфорилирования тиамина. Алкоголь нарушает всасывание всех витаминов в кишечнике и снижает печеночные запасы тиамина. Дефицит витаминов у алкоголиков связан с алиментарным фактором – недостаточно разнообразным питанием. У больных алкоголизмом лекарственные препараты, содержащие витамины, составляют важнейшую часть лечения. При этом необходимо длительное назначение препаратов, содержащих тиамин и пиридоксин. В открытом проспективном исследовании Е.А.Анисимовой (2001) изучалась эффективность бентиамина у мужчин, страдающих хроническим алкоголизмом. На фоне монотерапии бенфотиамином отмечено уменьшение болевого синдрома, редукция сенсорных, вегетативных и двигательных расстройств. Установлено увеличение скорости проведения по нервному волокну.
Безусловным показанием к назначению витаминных препаратов следует считать поражения черепных нервов различной этиологии. В клинической практике чаще всего комплексной терапии требует нейросенсорная тугоухость, неврит слухового нерва, невропатия лицевого нерва, невропатия зрительного нерва. В большинстве случаев в патогенезе невропатий черепных нервов существенную роль играют сосудистые факторы. Восстановление проведения по нервным стволам в этих случаях возможно при восстановлении микроциркуляции и длительном лечении витаминами группы В.
Относительно коротких курсов витаминной терапии требуют радикулопатии, связанные с вертеброгенными факторами. После устранения причин компрессии корешка, витамины группы В назначают на 2 – 3 недели, что в существенной мере ускоряет процесс реабилитации.
Препараты, содержащие витамины в необходимых пропорциях, широко представлены в продукции таких крупных производителей как корпорация . Все необходимые витамины содержит . Высокое содержание витаминов группы В отличает композицию Мультивитаминный комплекс пригоден как для профилактики поражений нервной системы, так и для лечебных программ. Из лекарственных средств в клинической практике нашли применение такие препараты как Мильгамма, нейромультивит.
Таким образом, лечение витаминами в комплексной терапии заболеваний периферической нервной системы не только не утратило своего значения, но получило более глубокое обоснование. Следует считать безусловным показанием назначение витаминов группы В во всех случаях повреждения нервной системы, в основе которых лежат процессы демиелинизации или нарушения ремиелинизации. Современная коррекция миелинопатий как системных обменных нарушений невозможна без своевременного и адекватного лечения препаратами, содержащими тиамин, пиридоксин и цианкобаламин. При заболеваниях, протекающих с нарушениями углеводного, жирового и белкового обмена (сахарный диабет) систематическое лечение витаминными препаратами необходимо для активации обменных процессов, восстановления процессов синтеза белковых соединений. Препараты, содержащие витамины совершенно необходимы для больных, страдающих от нарушений всасывания эссенциальных коферментов (алкоголизм, больные перенесшие сложные реконструктивные операции на органах желудочно-кишечного тракта).
Литература
1. Анисимова Е.И. Эффективность бенфотиамина в терапии алкогольной полиневропатии Журнал неврологии и психиатрии им. С.С.Корсакова. 2001. Т 12. № 101. С. 32-36.
2. Анциферов М.Б., Волкова А.К. Диагностика и лечение диабетической дистальной полинейропатии у больных сахарным диабетом в амбулаторной практике. РМЖ. 2008. Т. 16. № 15. С. 12 .- 15.
3. Зиновьева О.Е. Препараты альфа-липоевой кислоты в лечении диабетической полиневропатии. Неврология, психиатрия, нейросоматика. 2009. № 1. С. 58 – 62.
5. Mooney S., Leudorf J.E. Vitamin B6: a long known compound of surprising complexity. Molecules. 2009. T.14. p. 329 – 51.
Гиления лучше в снижении частоты рецидивов, чем такфидера или абаджио. Согласно исследованию Gilenya (финголимод) связана со значительно более низкими показателями рецидивов в годовом исчислении у пациентов с ремиттирующим рассеянным склерозом по сравнению с Tecfidera (диметилфумарат) или Aubagio (терифлуномид). Все три терапии показали схожее влияние на инвалидизацию.
Исследование «Сравнение финголимода, диметилфумарата и терифлуномида при рассеянном склерозе» было опубликовано в журнале неврология, нейрохирургия и психиатрия (Journal of Neurology , Neurosurgery , and Psychiatry ).
Пероральная иммунотерапия Novartis Gilenya , Biogen Tecfidera и Sanofi Genzyme Aubagio , в настоящее время является стандартной терапией для лечения РРС. Но хотя эти методы лечения эффективны для изменения активности РС, исследование, сравнивающее их эффективность между собой отсутствует. Для пациентов же с РС это очень важный момент, потому что если необходимо изменить препарат (например, из-за отсутствия толерантности), решение о более подходящей терапии должно основываться на научных данных.
Чтобы решить эту проблему, группа исследователей использовала международное обсервационное «когортное» исследование РС-а (an international observational MS cohort study ), идентифицировала пациентов с РРС, которых лечили Gilenya , Tecfidera или Aubagio и не менее трех месяцев.

Тремор - это непроизвольные, неконтролируемые движения частей тела.
Пациент может испытывать тремор как подергивание или дрожание, дрожащие движения. Тремор является распространенным симптомом, который встречается во многих неврологических состояниях, включая болезнь Паркинсона и РС. Он так же может появляться в семьях при отсутствии нейронных травм, заболеваний и предрасположенности. При рассеянном склерозе тремор обычно связан с атаксией, которая представляет собой проблему с координацией движений тела.
При рассеянном склерозе наиболее распространенным типом тремора является тремор намерения или мозжечковый тремор. Это тремор, который усиливается при использовании пораженной конечности, например, когда дрожит рука, если пациент достигает какого-либо предмета или пытается коснуться своего носа. У некоторых людей с РС может возникнуть постуральный тремор, это когда пациент удерживает определенную осанку, например, сидит в вертикальном положении.

Другое названия: натализумаб.
Тисабри - это препарат изменяющий течение рассеянного склероза (ПИТРС) для очень активного рецидивирующего-ремиттирующего РС.Пациент принимает Tysabri в виде внутривенной инфузии (капельница) один раз в четыре недели, препарат уменьшает количество и тяжесть рецидивов. Считается что тизабри уменьшает количество рецидивов примерно на 2\3 (70%) по сравнению с приемом плацебо.
Общие побочные эффекты препарата включают головокружение, тошноту, крапивницу (кожную сыпь) и дрожь.
Лечение при помощи Tysabri может увеличить риск прогрессирующей мультифокальной лейкоэнцефалопатии (PML) - редкой инфекции мозга, которая может привести к тяжелой инвалидности или даже смерти.
Рассеянный склероз – это еще одно свидетельство несовершенства нашей иммунной системы, которая иногда «сходит с ума» и начинает атаковать не внешнего «врага», а ткани собственного организма. При этом заболевании клетки иммунной системы разрушают миелиновую оболочку нервных волокон, которая образуется в процессе развития организма из определенного типа глиальных клеток – «служебных» клеток нервной системы. Миелиновая оболочка покрывает аксоны – длинные отростки нейрона, которые играют роль «проводов», по которым проходит нервный импульс. Сама же оболочка служит для электроизоляции, и в результате ее разрушения прохождение импульса по нервному волокну замедляется в 5-10 раз.
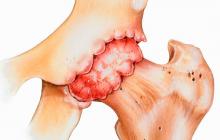
На фото по периферии бляшек видны скопления макрофагов (коричневая окраска). Макрофаги привлекаются в очаг поражения и активируются другими клетками иммунной системы – Т-лимфоцитами. Активированные макрофаги фагоцитируют («съедают») погибающий миелин, а, кроме того, сами способствуют его повреждению, продуцируя протеазы, провоспалительные молекулы, активные формы кислорода. (Иммуногистохимия, маркер макрофагов – CD68).
В норме клетки иммунной системы, как и другие клетки крови, не способны проникать непосредственно в нервную ткань – их не пускает так называемый гематоэнцефалический барьер. Но при рассеянном склерозе этот барьер становится проходимым: «сошедшие с ума» лимфоциты получают доступ к нейронам и их аксонам, где и начинают атаковать молекулы миелина, представляющего собой сложную многослойную белково-липидную структуру. Так запускается каскад молекулярных событий, приводящих к разрушению миелина, а иногда и самих аксонов.
Разрушение миелина сопровождается развитием воспаления и склерозированием пораженного участка, т.е. образованием соединительнотканного рубца в виде бляшки, замещающего миелиновую оболочку. Соответственно, в этом участке проводящая функция аксона нарушается. Бляшки расположены диффузно, рассеянно по нервной системе. Именно с таким расположением очагов поражения связано и само название болезни – «рассеянный» склероз, которая не имеет никакого отношения к обычной рассеянности (той, о которой мы иногда говорим в быту – «совсем склероз у меня, опять все забыл»).
Симптомы рассеянного склероза разнообразны, и зависят они от того, какие именно нервы поражены. Среди них – параличи, проблемы с равновесием, когнитивные нарушения, изменения в работе органов чувств (у четверти пациентов развитие заболевания начинается с нарушения зрения из-за неврита зрительного нерва).
Современное лечение рассеянного склероза оставляет желать лучшего.
Эффективного лечения пока не существует, тем более что причины, вызывающие это заболевание, до сих пор не известны, имеются лишь данные о возможном влиянии среды и генетической предрасположенности. Для лечения помимо симптоматической терапии, позволяющей снять боль и уменьшить спазмы мышц, используются препараты глюкокортикоидов для снижения воспаления, а также иммуномодуляторы и иммунодепрессанты, направленные на подавление «плохой» активности иммунной системы. Все эти средства способны замедлить развитие заболевания и снизить частоту обострений, но не излечивают пациента полностью. Не существует и лекарств, способных восстанавливать уже поврежденный миелин.
Однако такое лекарство, направленное именно на восстановление миелина, а не только на замедление патологического процесса, вскоре может появиться. Разработка под рабочим названием Anti-LINGO-1 от швейцарской компании «Biogen», крупнейшего производителя препаратов для терапии рассеянного склероза, сейчас проходит 2 фазу клинических испытаний. Препарат представляет собой моноклональное антитело, способное специфично связываться с белком LINGO-1, который препятствует процессу миелинизации и формированию новых аксонов. Соответственно, если этот белок «выключить», миелин начинает восстанавливаться.
В опытах на животных использование нового препарата приводило к 90-процентной ремиелинизации. У пациентов с рассеянным склерозом, принимающих Anti-LINGO-1, на текущий момент отмечается улучшение проводимости зрительного нерва. Однако полные результаты клинических испытаний на больных будут получены только к 2016 г.
Аксон
Аксон - одиночный отросток нервной клетки, достигающий в длину до 1,5 метра, постоянного диаметра, покрытый нейроглиальными оболочками. Аксон проводит нервные импульсы от тела нервной клетки к другим нейронам или к рабочим органам. В месте, где аксон отходит от тела, имеется аксонный холмик , который, сужаясь, переходит в начальный сегмент аксона, ещё не покрытый нейроглиальной оболочкой. В аксонном холмике отсутствует вещество Нисля.
Клеточная мембрана аксона называется аксолеммой , а цитоплазма - аксоплазмой . Аксолемма выполняет важнейшую роль в проведении нервного импульса. В аксоплазме находятся нейрофибриллы, митохондрии и агранулярная ЭПС. Все эти органеллы сильно вытягиваются вдлину. В аксоплазме происходит постоянный ток молекул от тела нейрона к периферии и в обратном направлении.
Аксон делится на несколько крупных ветвей , которые отходят от перехватов Ранвье. Эти ветви оканчиваются многочисленными разветвлениями - терминалями . Они образуют синапсы на других ннейронах.
Аксон всегда покрыт нейроглиальной оболочкой. В зависимости от характера структуры оболочек различают 2 типа волокон :
1) немиеленизированные (безмякотные);
2) меилинизированные (мякотные).
Немиелинизированные волокна главным образом встречаются в вегетативной нервной системе и имеют малый диаметр. Такой аксон погружён в нейроглиальную клетку так, что оболочка нейроглиальной клетки смыкается над аксоном, охватывает его со всех сторон, образуя мезаксон .
Установлено, что в одну нейроглиальную клетку может погружаться до 10-20 аксонов. Такие волокна называются волокнами кабельного типа . При этом оболочку образует цепочка нейроглиальных клеток.
Второй тип волокон называется немиелинизированными. Они имеют больший диаметр аксона.
Нейроглиальная оболочка состоит из двух слоёв: внутренний слой - миелиновая оболочка, наружный слой - неврилемма .
Протяжённость миелиновой оболочки начинается, несколько отступив от тела аксона, и заканчивается на расстоянии 2 мкм от синапса. Она состоит из сегментов равной длины - межузловых сегментов , разделённых перехватами Ранвье. Здесь аксон либо обнажён, либо покрыт неврилеммой. В области перехватов Ранвье могут отходит ветви. Миелиновая оболочка - упорядоченная структура, которая состоит из чередующихся белковых и липидных слоёв. Её структурной единицей является бимолекулярный липидный слой, заключённый между двумя молекулярными белковыми слоями. Толщина этой субъединицы равняется 115-130 А, а количество самих слоёв может достигать 100 и более. Миелиновая оболочка является изолятором и обладает большим сопротивлением постоянному току, что способствует огромному ускорению проведения нервного импульса. Нервный импульс как бы перескакивает с одного перехвата Ранвье на другой, так как деполяризация аксонов происходит только в областях перехватов Ранвье. Такое проведение нервного импульса называется сайтоторным (скачкообразным).